Advanced Science:心脑轴全新研究成果M1兴奋性神经元调控心脏功能
2024-05-10

文章题目:Manipulation of Glutamatergic Neuronal Activity in the Primary Motor Cortex Regulates Cardiac Function in Normal and Myocardial Infarction Mice
发表时间:2024-03-15
发表期刊:Advanced Science
研究团队:陕西师范大学体育学院田振军团队和生命科学学院青年教师贺志雄
众所周知,心脏的活动和功能是由复杂的神经网络控制的,该网络涉及某些皮质和皮质下前脑区域。心-脑间互相沟通相互影响,如岛叶皮层的刺激可改变心脏功能。同时,皮层损伤可能导致心脏问题,但具体影响心脏功能的神经元细节仍需明确。初级运动皮层(M1)不仅在运动执行中起主导作用,还参与高级认知功能和疼痛调节。M1与心脏的联系已通过使用PRV追踪证实,但M1调控心脏功能的具体机制和路径还需进一步探索。
2024年3月15日,陕西师范大学体育学院田振军团队和生命科学学院青年教师贺志雄在Advanced Science上发表题为“Manipulation of Glutamatergic Neuronal Activity in the Primary Motor Cortex Regulates Cardiac Function in Normal and Myocardial Infarction Mice”的研究,研究通过病毒示踪、fMOST三维成像、光遗传学、化学遗传学和钙成像等技术发现小鼠初级运动皮层(M1)谷氨酸能神经元影响心脏功能,明确了下游中缝核(MnR)为M1回路中影响心脏功能的关键中继脑区之一,同时构建心肌梗死(MI)模型验证了病理状态下M1神经元活动对心脏功能的影响。该研究为深入分析脑与心的确切关系提供了重要证据,为研究脑心综合征的发病机制和治疗提供了新思路。
01 研究结果
研究人员首先在左、右心室壁注射PRV-EGFP和PRV-mRFP,利用fMOST进行小鼠全脑三维重建,发现M1脑区存在EGFP和mRFP共标,表明 M1 区域的神经元可能同时控制左心室和右心室的心肌活动。
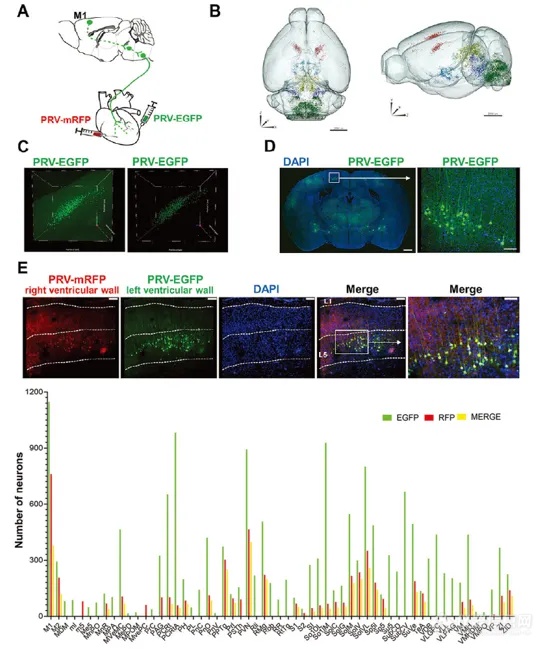
图1. 利用fMOST对心源性注射伪狂犬病病毒的小鼠进行全脑成像
研究人员进一步通过光遗传学激活、化学遗传学失活和消融来操纵M1谷氨酸能神经元发现:M1兴奋性神经元通过光遗传激活显着增加心率(HR)、左心室射血分数(LVEF)、左心室缩短分数(LVFS)、增加收缩压(SBP)、舒张压(DBP)和平均动脉压(MAP);化学遗传抑制则抑制M1神经元可显着降低心率、心功能和血压;利用Caspase3消融谷氨酸能神经元降低心功能和血压,而不改变心率。
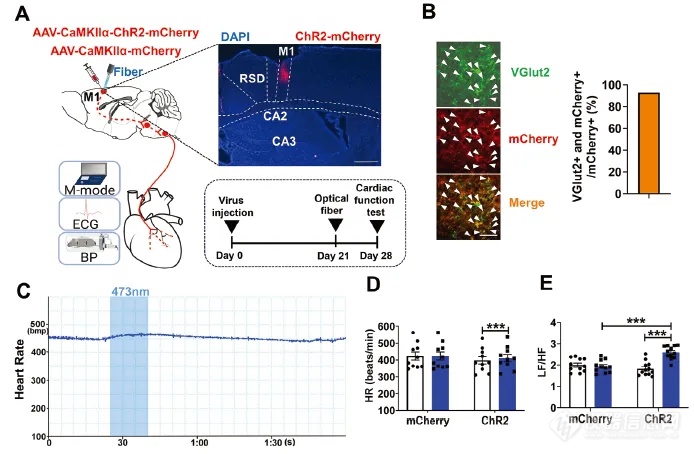
图2. 激活 M1 谷氨酸能神经元会影响心脏功能和血压
为研究M1投射下游脑区,研究人员进一步利用病毒示踪技术发现M1谷氨酸能神经元向MnR的强烈投射,且MnR中的色氨酸羟化酶2(TPH2)阳性神经元接近M1投射纤维,然后利用光遗传和钙成像相结合证实了MnR神经元接收来自M1的直接输入。
研究人员通过光遗传激活M1突触后MnR神经元,发现小鼠心率显著增加、心脏功能增强、血压显著升高。同时仅光遗传激活M1谷氨酸能神经元就足以影响心脏功能、血压和自主神经活动的平衡,MnR注射xx可取消光遗传激活效应,表明MnR神经元对于M1引起心脏活动是必要的。
研究人员进一步在病理状态下研究M1谷氨酸能神经元对心脏功能的影响,通过构建心肌梗死(MI)模型小鼠,光遗传激活M1谷氨酸能神经元,显著增加心率,对MI小鼠心脏功能产生不利影响。对MI小鼠的化学遗传抑制和Caspase3消融也进一步证实了M1兴奋性神经元参与MI后心脏功能的调节。
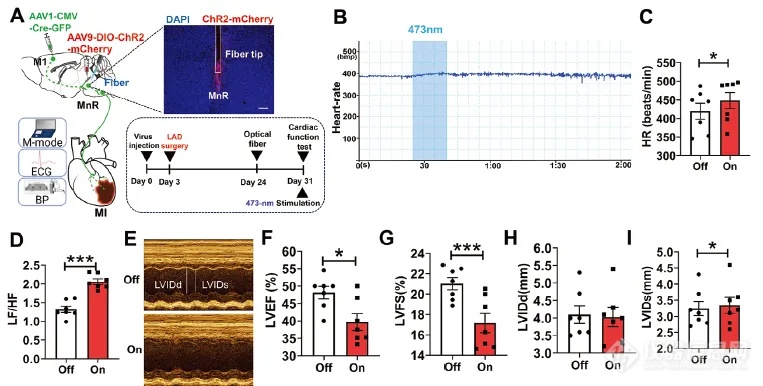
图3. M1- MnR 神经元光遗传激活影响MI模型小鼠的心脏功能
最后,在MI小鼠的M1突触后MnR神经元和M1神经元分别进行光遗传激活均影响MI小鼠的心脏功能和血压。
以上结果表明操纵M1神经元活动影响正常小鼠的心率、心脏功能和血压,也可以影响病理条件下小鼠的心脏活动。
02 全文总结
在这篇研究中,研究人员利用病毒示踪、fMOST三维成像、钙成像和遗传学技术对小鼠大脑影响心脏活动的机制进行探索,发现M1中特定兴奋性神经元群与小鼠心脏功能相关,激活这些神经元可增加心率、射血分数和血压,而抑制它们则会降低心脏功能和血压。发现中缝核(MnR)作为M1回路中的关键中继脑区域之一,影响心脏功能。通过建立心肌梗死(MI)模型,发现病理状态下M1神经元同样可调节心脏功能。这些结果证实了M1神经元在心脏功能和血压调节中的重要性,为理解心血管调节的神经机制提供了新见解。
原文链接:https://doi.org/10.1002/advs.202305581
2024
/
05-10
所属分类:
学术进展
相关资讯—

